Tous droits réservés © NeurOreille (loi sur la propriété intellectuelle 85-660 du 3 juillet 1985). Ce produit ne peut être copié ou utilisé dans un but lucratif.
Pour demain, les progrès technologiques vont forcèment déboucher sur des améliorations des appareils prothétiques (aides auditives, implants), qui devraient rester, pour longtemps encore, le mode de réhabilitation le plus utilisé.
Mais on peut aussi prédire une percée de la pharmacologie locale (transtympanique) pour protéger les cellules ciliées et les neurones, retarder leur dégénérescence et traiter les acouphènes.
Et pour "après-demain", pourquoi ne pas envisager ... la régénération des cellules ciliées à l'aide de thérapies cellulaire ou génique ?
Régénération des cellules ciliées ?
Pour l'instant, et probablement pour des années, la régénération des cellules ciliées de la cohlée humaine va rester un rêve ... inaccessible ? Qui sait ? En tout cas, des équipes de recherche sont sur la voie, encouragées par des résultats probants obtenus notamment sur des cochlées d'oiseaux ...
Une grande majorité des surdités acquises est liée à la dégénérescence des cellules ciliées. Schématiquement, on passe par les 3 stades : organe de Corti normal / destruction et disparition des cellules ciliées et des cellules support / monocouche de cellules non différenciées.
Dégénérescence de l'organe de Corti (S. Blatrix, d'après J. Stone)
Le défi de la régénération est maintenant d'inciter cette monocouche cellulaire à développer un nouvel organe de Corti fonctionnel : de nouvelles cellules ciliées qu'il faudra alors aider à se reconnecter au cerveau.
L'animation ci-dessous schématise les deux directions de recherche.
La thérapie génique consiste à tenter de « réveiller », avec des molécules appropriées, quelques cellules souches dormantes qui peuvent se trouver dans la monocouche cellulaire, pour les faire développer en cellules ciliées.
La thérapie cellulaire consiste à tenter la greffe de cellules souches embryonnaires dans la cochlée, puis de les aider à se différencier en cellules ciliées pour prendre la place des cellules manquantes.
Dans les deux cas, le challenge est de taille et l'on ne peut encore ni prédire le succès, ni bien sûr donner une date, pour une éventuelle application thérapeutique !
Autres applications des thérapies cellulaire et génique ?
Dans l'attente d'un hypothétique succès des recherches évoquées ci-dessus, on peut imaginer un avenir plus proche à d'autres applications des thérapies cellulaire et génique. En particulier, la connaissance des gènes impliqués dans de nombreuses surdités progresse constamment : on peut donc envisager de futures thérapies permettant de corriger le gène défectueux, afin de rétablir le fonctionnement du système auditif.
Vers une pharmacologie locale et spécifique ...
On connaît désormais de mieux en mieux les mécanismes biologiques et moléculaires responsables des atteintes cellulaires de la cochlée.
On peut donc de mieux en mieux cibler la protection ou la résistance des cellules sensorielles ou des neurones cochléaires.
Actuellement, le principal obstacle à la mise en œuvre d'essais cliniques chez l'homme réside dans les effets secondaires potentiels des molécules candidates, si elles sont délivrées par voie générale.
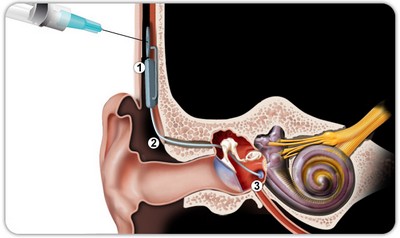
Une administration locale, c'est-à-dire directement sur la fenêtre ronde (schéma), de ces molécules efficaces est réalisable !
| S. Blatrix, d'après J-L. Puel |
Système de mini-pompe implantable
|
L'arrivée sur le marché de plusieurs systèmes de délivrance (cathéter, seringue etc.) laisse entrevoir des possibilités thérapeutiques prometteuses pour la réalisation de traitements aigus. Ces dispositifs sont déjà utilisés pour traiter les vertiges !
Des moyens plus sophistiqués comme l'implantation d'un pompe rechargeable à travers la peau pourraient être envisagés.
Expérimentalement, chez l'animal, des succès probants ont déjà été obtenus pour bloquer pharmacologiquement la dégénérescence des cellules sensorielles, ou même pour stopper des acouphènes. Alors, pourquoi pas bientôt chez l'homme ?
... couplée aux appareillages et implants ?
Et pourquoi ne pas envisager une mini pompe, délivrant une molécule protectrice, couplée avec un implant cochléaire ?
L'objectif serait de maintenir un maximum de neurones en vie, gage de bonnes performances de l'implant cochléaire.
On pourrait de même envisager de coupler les aides auditives avec une thérapie protectrice, pour ralentir la dégénérescence des cellules sensorielles et des neurones, dans les traitements de la presbyacousie par exemple ?
 Français
Français
 English
English
 Español
Español
 Português
Português


Facebook Twitter Google+